|
2019; 7 (1): |
Gelbfieber, Tollwut, Japanische Enzephalitis, Typhus, Meningokokken
1Institut für Spezifische Prophylaxe und Tropenmedizin, Medizinische Universität Wien, Referenzzentrale für Impfungen, Reise- und Tropenmedizin des Ministeriums für Arbeit, Soziales, Gesundheit und Konsumentenschutz; 2Zentrum für Reisemedizin, Wien; 3Institut für Hygiene, Mikrobiologie und Umweltmedizin, Medizinische Universität Graz; 4Swiss Tropical and Public Health Institute, Basel; Infektiologie und Spitalshygiene, Kantonsspital, St. Gallen; 5traveldoc, Wien; 6Zentrum für Virologie, Medizinische Universität Wien; 7Universitätsklinik für Dermatologie und Venerologie, Medizinische Universität Innsbruck; 8FA für Kinderheilkunde, St. Marein im Mürztal; 9Klinische Abteilung für Infektionen und Tropenmedizin, Universitätsklinik für Innere Medizin I, Medizinische Universität Wien; 10Universitätsklinik für Innere Medizin II (Infektiologie, Immunologie, Pneumologie, Rheumatologie), Medizinische Universität Innsbruck; 114. Medizinische Abteilung mit Infektiologie, SMZ Süd KFJ-Spital der Stadt Wien
Neue Empfehlungen der Weltgesundheitsorganisation (WHO) bezüglich der Impfungen gegen Gelbfieber und gegen Tollwut haben zu Diskussionen in Fachkreisen und in der Folge zu unterschiedlichen Vorgangsweisen in mehreren europäischen Ländern geführt.
Um keine Verunsicherung bei Ärzteschaft wie auch Reisenden zu erzeugen, ist das Ziel dieses Expertenstatements (erstellt von der Österreichischen Gesellschaft für Vakzinologie in Kooperation mit der Referenzzentrale für Impfungen des Sozialministeriums [ISPTM, MedUniWien], der Österreichischen Gesellschaft für Infektionskrankheiten und Tropenmedizin und der Österreichischen Gesellschaft für Tropenmedizin, Parasitologie und Migrationsmedizin), eine Harmonisierung der Impfempfehlungen auf der Basis der vorliegenden wissenschaftlichen Evidenz sowie von fachlichen / theoretischen Überlegungen einheitlich für Österreich zu erarbeiten. Abgesehen von den genannten zwei Impfungen gehören auch Impfungen gegen Japanische Enzephalitis, Typhus und Meningokokken zu den Reiseimpfungen mit speziellen Indikationsstellungen, die ebenso immer wieder zu unterschiedlichen Empfehlungen und Vorgangsweisen geführt haben.
Die in der Folge erarbeiteten Empfehlungen sollen daher als Ergänzung zu den im Österreichischen Impfplan beschriebenen Reiseimpfungen verstanden werden.
1.1 Epidemiologie
Relativ rezente Ausbrüche von Gelbfieber („Yellow Fever“ – YF) in Angola [1], Brasilien [2] und anderen südamerikanischen Ländern zeigen, dass YF in Endemiegebieten nach wie vor ein Problem darstellt. Dazu kommt noch, dass die Inzidenz humaner Gelbfieberfälle durch Impfaktionen im Land beeinflusst wird [3] und somit das tatsächliche Risiko für Reisende nicht immer direkt von den Erkrankungszahlen der Lokalbevölkerung abgeleitet werden kann.
Weiters wurden bei dem Ausbruch in Angola 2016 einige ungeimpfte chinesische Arbeiter angesteckt, was auf die Gefahr hinweist, dass YF auf den asiatischen Kontinent übertragen werden könnte, der zwar zurzeit frei von YF ist, wo es aber geeignete Vektoren in reicher Zahl gäbe [1].
Alleine in Südamerika sind zwischen August 2016 und August 2018 mindestens 13 ungeimpfte europäische Reisende an Gelbfieber erkrankt, während es zwischen 1999 und August 2016 nur insgesamt sechs Fälle bei Touristen in ganz Südamerika gab [4 – 6]. Dies zeigt eine für die Reisemedizin gravierende Änderung der epidemiologischen Verhältnisse.
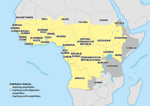
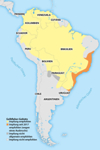
Die folgenden Abbildungen zeigen Karten zur Verbreitung von YF und zu den WHO-Impfempfehlungen für Afrika (Abb. 1a) und Südamerika (Abb. 1b).
|
Abbildung 1a: Gelbfieber in Afrika
Quelle: modifiziert nach [7]
Click on the figure icon to see higher resolution |
|
Abbildung 1b: Gelbfieber in Südamerika
Quelle: modifiziert nach [7]
Click on the figure icon to see higher resolution |
1.2 Impfstoffe
Der seit vielen Jahren verfügbare Impfstoff (Stamaril®) ist ein auf Hühnerembryonen gezüchteter 17D-Lebendvirus-Impfstoff, der eine ausgezeichnete Immunantwort auslöst und in der Regel kaum krankmachende Eigenschaften besitzt. Er kann ab dem vollendeten 9. Lebensmonat eingesetzt werden (in Ausnahmefällen Zulassung ab dem 6. Lebensmonat).
Als Kontraindikationen gelten Hühnereiweißallergie, Dysfunktion der Thymusdrüse,
Myasthenia gravis sowie Fieber
1.3 Nebenwirkungen
Trotz allgemein guter Verträglichkeit der Gelbfieberimpfung kann es selten, aber doch bei bestimmten Personengruppen zum Auftreten schwerer Nebenwirkungen kommen. Diese Tatsache führte dazu, die Impfindikation strenger zu stellen und auch die tatsächliche Schutzdauer zu hinterfragen.
Entsprechend präzisen Beschreibungen sind schwere viszerotrope (AVD) oder neurotrope (AND) Nebenwirkungen
nach Gelbfieberimpfung möglich. In einer Studie wurde die Inzidenz dieser Nebenwirkungen mit
1.4 Impfung
Mit 11. Juli 2016 hat die WHO den Beschluss gefasst, die Gültigkeitsdauer einer Gelbfieberimpfung von „zehn Jahre“ auf „lebenslang“ anzuheben [12, 13].
Laut dem „Yellow Book 2018“ der US-amerikanischen „Centers for Disease Control and Prevention“ (CDC) werden einige Personengruppen bzw. Umstände definiert, bei denen von der einmaligen, lebenslang gültigen Gelbfieberimpfung abgewichen werden sollte [7]:
- Personen, denen die Erstimpfung im Kleinkindesalter (< 2 Jahre) oder während einer Schwangerschaft, unabhängig vom Schwangerschaftstrimester, verabreicht wurde, sollten vor einer Reise in ein Risikogebiet eine weitere Impfung erhalten.
- Wenn die Gelbfieberimpfung gleichzeitig mit einer weiteren Lebendimpfung wie MMR gegeben wird, kann dies die Dauer des Impfschutzes verringern, und eine Gelbfieberimpfung sollte (wie bis dato) nach zehn Jahren erneut gegeben werden.
- Ebenso sollten Empfänger einer hämatologischen Stammzelltransplantation (HSCT), die vor der HSCT eine Gelbfieberimpfung erhalten haben, nach der HSCT – sobald sie ausreichend immunkompetent sind (Mindestabstand zwei Jahre) – eine weitere Gelbfieberimpfung bekommen, sofern sie in Risikogebiete fahren.
- HIV-infizierte Personen sollen alle zehn Jahre erneut geimpft werden (eventuell auch in kürzeren Intervallen), sofern sie ein Gelbfieberrisiko haben.
- Schließlich sollte auch bei Laborpersonal, das mit Wildtyp-Gelbfiebervirus zu tun hat, alle zehn Jahre ein Antikörperstatus (NT IgG) gemacht und falls nötig aufgefrischt werden.
- Reisende, die planen, eine längere Zeit in einem Endemiegebiet zu verbringen oder in besonders hochendemische Gebiete wie das ländliche Westafrika zu fahren (insbesondere während der Jahreszeit mit den höchsten Übertragungsraten) oder sich in einem Ausbruchsgebiet aufzuhalten, sollten mit einer weiteren Impfung aufgefrischt werden.
Letztere Empfehlung des Yellow Book scheint auf den ersten Blick im Gegensatz zur oben beschriebenen WHO-Empfehlung zu stehen. Allerdings muss in Erinnerung behalten werden, dass die WHO-Empfehlungen primär Menschen in Endemiegebieten betreffen und nicht Reisende, die eine verhältnismäßig kleine Risikoklientel darstellen.
Darüber hinaus gibt es für die lebenslange Schutzwirkung der Gelbfieberimpfung nach einer einzelnen Impfdosis bei Reisenden aus Nicht-Endemiegebieten keine belastbaren Daten, wie auch jüngst eine detaillierte Recherche des kanadischen CATMAT belegt [14]. Die meisten Teilnehmer an den Studien zu diesem Thema stammten entweder aus Endemiegebieten oder hatten lang dort gelebt, so dass eine Boosterung der Impfantwort durch natürliche Exposition nicht auszuschließen ist. Auch die Analysemethoden, mit denen die Immunantwort nach Gelbfieberimpfung gemessen wurde, waren unterschiedlich.
Eine Studie von Niedrig et al. zeigte, dass nach 17D-Gelbfieberimpfung in den Jahren 2 bis 10
bereits
Eine weitere rezente Studie zeigt nun sehr deutlich, dass bei gesunden Reisenden, die vor mehr als zehn Jahren
(Bereich zwischen 10 und 53 Jahren; im Mittel 15 Jahre) gegen Gelbfieber geimpft wurden, nur mehr
Dokumentierte Impfversager nach Gelbfieberimpfung sind hingegen bisher ausnahmslos innerhalb der Zehn-Jahres-Frist nach der Impfung beobachtet worden und nicht erst später, wie die WHO bereits festgestellt hat [13]. Diese Daten deuten auf ein primäres Versagen des Angehens der Impfung hin, ein Phänomen, das bei allen Lebendimpfungen vorkommen kann [17].
In einer brasilianischen Studie zeigte sich die Abnahme der Seroprotektionsrate von
Für eine adäquate Immunantwort nach Kontakt mit dem YF-Virus ist auch eine
Somit liegen zusammenfassend keine klaren Daten bei großen Kollektiven – vor allem aber bei Reisenden – vor, die generell eine lebenslange Schutzwirkung der Gelbfieberimpfung untermauern würden [14].
Neben den medizinischen / immunologischen Überlegungen zur Validität einer einmaligen, lebenslang geltenden Gelbfieberimpfung können auch logistische Probleme bei der Einreise in das Zielland auftreten, da noch längst nicht alle Staaten (vor allem in Afrika) die neue Regelung akzeptieren. Einreiseprobleme können daher auftreten, wenn die Gelbfieberimpfung mehr als zehn Jahre zurückliegt und vor Einreise keine Auffrischung verabreicht wurde (es empfiehlt sich eine Anfrage in der zuständigen Botschaft).
1.5 Empfehlungen
- Personen, die bereits eine Gelbfieberimpfung erhalten haben, sollten nach Ablauf von zehn Jahren erneut
eine Impfung erhalten, sofern sie eine Reise in ein rezent aktives Endemiegebiet planen. Die Definition
dieser Gebiete ist den jeweils aktuellen Karten (
z. B. der WHO) zu entnehmen (s. Punkt 1.1). Dies gilt in besonderem Maß für:- Personen, die zeitgleich mit der Gelbfieberimpfung eine Lebendimpfung erhalten haben
- Kinder, die vor dem zweiten Geburtstag erstmalig geimpft wurden
- Frauen, die während der Schwangerschaft geimpft wurden
- HIV-Infizierte (cave CD4+-Zellzahl)
- Personen nach Stammzelltransplantation, sofern seit der Transplantation mehr als zwei Jahre verstrichen sind und der Patient immunologisch unauffällig ist
- Personen, die nach Gelbfieberimpfung eine starke immunsuppressive Therapie erhalten haben und sich wieder in einem immunkompetenten Zustand befinden
- Personen, die unter geringgradiger Immunsuppression (
z. B. Kortisontherapie) geimpft wurden
- Personen, die noch keine Impfung erhalten haben, werden im Einklang mit den WHO-Empfehlungen zunächst einmal gegen Gelbfieber geimpft. Da die Datenlage für eine nur einmalige Impfung nach dem WHO-Schema derzeit relativ gering ist, sollte bei dieser Gruppe das weitere Vorgehen erst zehn Jahre nach der Erstimpfung entschieden werden, da vermutlich zu diesem Zeitpunkt bereits mehr Langzeitdaten vorliegen werden.
- Darüber hinaus kann als Entscheidungshilfe, ob eine Boosterung erfolgen soll, ein Neutralisationstest (NT) angeboten werden; dies vor allem bei Personen mit fraglichem Impferfolg infolge möglicher (geringgradiger) Immunsuppression oder entsprechender Umstände (siehe oben).
- Bei unklaren Einreisevorschriften (kann an der jeweiligen Botschaft erfragt werden) kann eine erneute Impfung nach zehn Jahren empfehlenswert sein.
- Eine erneute Impfung nach zehn Jahren ist bei jenen Personen, die diese Impfung nur aus formalen Gründen (Einreisebestimmungen in Länder ohne Gelbfieberrisiko, Kreuzfahrten etc.) erhalten haben, nicht vorgesehen.
2.1 Epidemiologie
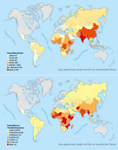
In Westeuropa konnte die Tollwut durch groß angelegte Impfaktionen für Füchse weitgehend zurückgedrängt werden. Österreich (und ganz Westeuropa) wurde 2008 von der WHO für tollwutfrei erklärt. Dies gilt jedoch nicht für Ost und Südosteuropa, und es gilt nur für die sogenannte klassische oder terrestrische Tollwut, die in Europa in erster Linie von Füchsen übertragen wurde. Die großen Problemareale der Tollwut liegen in Asien, Afrika und Teilen von Südamerika (siehe Abb. 2).
|
Abbildung 2: Tollwutverbreitung weltweit
Quelle: modifiziert nach [21] Click on the figure icon to see higher resolution |
Daneben gibt es jedoch auch die Fledermaus-Tollwut, die in Westeuropa vereinzelt noch vorkommen kann, vor allem aber in Afrika und Südamerika auftritt.
Epidemiologisch gibt es zwei Formen der terrestrischen Tollwut:
- die sogenannte sylvatische Wut mit dem primären Zyklus Fuchs zu Fuchs, wobei andere Tiere oder auch der Mensch nur selten angesteckt werden, und
- die urbane Wut mit dem primären Zyklus Haushund zu Haushund, bei dem es viel häufiger zu menschlichen Ansteckungen kommt, wenn der Mensch in engem Kontakt mit dem domestizierten Tier lebt. Dieser Typ ist vor allem in ressourcenarmen Ländern vorherrschend.
Weltweit sterben jährlich mindestens 50.000 Menschen an Tollwut [22]. In großen Teilen Afrikas, Lateinamerikas und Asiens ist das Ansteckungsrisiko dementsprechend hoch [23].
2.2 Impfstoffe
Von den modernen Gewebekulturimpfstoffen ist derzeit nur Rabipur® in Österreich
zugelassen. Andere Impfstoffe wie Imovax rabies® Human-Diploid-Cell-Vaccine oder
Tollwut-Impfstoff Mérieux® können allenfalls über die internationale Apotheke
bestellt werden (
Bei Rabipur® handelt es sich um ein auf Hühner-Embryonalzellen gezüchtetes, inaktiviertes Tollwut-Virus (Stamm Flury LEP), das Spuren von Antibiotika enthält.
Die Impfung kann bei Kindern jeden Alters und Erwachsenen verwendet werden. Sie wird laut Zulassung i.m. in den M. deltoideus (bei Kindern unter zwei Jahren anterolateral in den Oberschenkel) appliziert und soll nicht intragluteal, intravasal oder subkutan verabreicht werden. Eine intradermale Applikation ist jedoch zulässig, siehe unten.
2.3 Impfschemata
Die Zulassung von Rabipur® umfasst folgende präexpositionelle Schemata zur
intramuskulären Anwendung:
Tag 0 – 7 – 21/ 28 oder ein
Kurzschema: Tag 0 – 3 – 7.
Seit 2017 empfiehlt die WHO [24] für die präexpositionelle Impfung nur noch zwei
Teilimpfungen. Diese werden an den Tagen 0 und 7 verabreicht. Dazu existiert erst eine einzige Publikation
[25] (zu Details aus dieser Studie siehe weiter unten). Darüber hinaus ist laut WHO die
intramuskuläre mit der intradermalen Applikation in der Wirksamkeit vergleichbar (Letztere hat den
Vorteil des geringeren Impfstoffverbrauchs). Eine intradermale Dosis entspricht 0,1 ml (max.
0,2 ml), eine intramuskuläre Dosis 1,0 ml (
Obwohl dieses Schema in erster Linie für ressourcenarme Länder entwickelt wurde, um Impfstoff so ökonomisch wie möglich einzusetzen, wird es von der WHO ausdrücklich auch für Reisende empfohlen. In Anbetracht entsprechender Studien [25] und der Tatsache, dass bei entsprechender Exposition in jedem Fall erneut zwei Impfungen durchgeführt werden müssen, lässt sich ein reduziertes präexpositionelles intradermales Impfschema sicherlich rechtfertigen.
Soentjens et al. verglichen in einer Studie mit 500 gesunden Erwachsenen ein Zwei-Dosen-Schema mit
einem Drei-Dosen-Schema der Tollwutimpfung [25]. Die Probanden erhielten entweder jeweils
zwei i.d. Dosen von 0,1 ml Impfstoff an den Tagen 0 und 7 oder das damalige Standardschema mit einer
Dosis von 0,1 ml i.d. an den Tagen 0, 7 und 28. Es handelte sich um eine
Nichtunterlegenheits-(„Non-Inferiority“)-Studie. Ein bis drei Jahre nach der
Grundimmunisierung erhielten die Teilnehmer eine Boosterdosis von einmal 0,1 ml i.d., um die
Boosterbarkeit zu testen. Der primäre Endpunkt bestand im Prozentsatz jener Personen, die sieben
Tage nach der Boosterung einen adäquaten Antikörperspiegel von
2.4 Kontraindikationen und Nebenwirkungen
Als Kontraindikationen für die präexpositionelle Gabe gelten schwere Überempfindlichkeit gegenüber
Impfstoffbestandteilen und schwere fiebrige Erkrankungen. Bei klinisch manifester und schwerer
Hühnereiweißallergie sollte präexpositionell ein nicht auf Hühnereibasis
produzierter Impfstoff bevorzugt werden (
Für die postexpositionelle Prophylaxe wird aufgrund des letalen Verlaufs der Erkrankung auf keine Kontraindikationen eingegangen.
An Nebenwirkungen sind möglich: lokale Schmerzen und Verhärtungen an der Stichstelle, Fieber, Schüttelfrost, Kopfschmerzen, Hautreaktionen (Überempfindlichkeit bis Schock), angstbedingte Reaktionen, Myalgie, Arthralgie, gastrointestinale Störungen, sehr selten Enzephalitis oder Guillain-Barré-Syndrom.
2.5 Ziele der Tollwutimpfstrategie
Tabelle 1 zeigt die Ziele, die mit einer Tollwutimpfung erreicht werden müssen.
|
Tabelle 1: Begründung und Ziele der „neuen“ Tollwutimpfstrategie
Quelle: Hatz C |
Von diesen Punkten ist die – möglichst lebenslange – Boosterbarkeit und damit der sichere Schutz nach Auffrischungsimpfung im Fall einer Exposition zweifellos der wichtigste.
Bezüglich der Boosterbarkeit nach längerer Zeit ist auf die Studien von Suwansrinon et al. [26] und Khawplod et al. [27] zu verweisen. Sie untersuchten prospektiv Personen, die eine prä- oder postexpositionelle Rabiesimpfung mit Gewebekultur-Impfstoffen i.d. oder i.m. erhalten hatten. Die Impfungen lagen fünf bis 21 Jahre zurück. Zu Beginn der Studie waren bei allen Probanden messbare Spiegel neutralisierender Antikörper vorhanden. Sie erhielten dann einen Booster von 0,1 ml Impfstoff i.d. an den Tagen 0 und 3. Neutralisierende Antikörper wurden an den Tagen 5, 7 und 14 bestimmt. Alle bis auf einen Probanden zeigten eine beschleunigte Antikörperantwort nach den beiden Boostern. Im Mai 2018 erschien ein systematischer Review zur Boosterbarkeit nach Tollwutimpfung [28], der 36 Studien inkludierte, von denen 19 für eine Metaanalyse geeignet waren. Die Antikörperspiegel nach primärer Impfung mit einem i.d. Schema waren niedriger als nach i.m. Applikation, in beiden Fällen war jedoch auch nach langer Zeit eine adäquate Boosterbarkeit gegeben.
Es gibt auch Daten – allerdings aus kleineren Studien mit einem nicht sehr breiten Altersspektrum (cave
Primärimmunisierung bei Personen
Das Schweizerische Expertenkomitee für Reisemedizin hat eine gegenüber der WHO-Empfehlung etwas modifizierte Impfempfehlung abgegeben [31]. Demnach sollen für die Grundimmunisierung zwei Impfungen im Abstand von ≤ 28 Tagen (mindestens jedoch im Abstand von 7 Tagen) gegeben werden. Dabei gilt: Je näher das Intervall an die idealen 28 Tage kommt, desto höher dürfte der resultierende Antikörperspiegel sein. Die i.m. Applikationsroute wird der intradermalen vorgezogen.
Bei immunkompromittierten Personen wird explizit das bisherige Standardschema mit Impfungen an den Tagen 0 – 7 – (21 / 28) empfohlen.
Nach einem Jahr oder später –
2.6 Empfehlungen
- Die prinzipielle Empfehlung der zugelassenen präexpositionellen Tollwutimpfschemata an den Tagen 0 – 7 – 21 oder 0 – 3 – 7 bleibt weiterhin aufrecht.
- Für die präexpositionelle Tollwutprophylaxe bei Reisenden können alternativ gemäß der WHO-Empfehlung zwei Impfungen an den Tagen 0 – 7 oder 0 – 28 (Beobachtungen zeigen, dass ein größeres Intervall zu höheren Titern führt) empfohlen werden und eine Auffrischung nach einem Jahr bzw. vor möglicher Exposition (Begründung: immunologische Überlegungen, um langlebige Plasma- und Memory-Zellen zu erhalten) [27].
- Als primäre Applikationsroute wird die intramuskuläre Verabreichung empfohlen. Eine intradermale Verabreichung ist alternativ möglich und gleichwertig (und hat den Vorteil, Impfstoff zu sparen, was bei Versorgungsengpässen günstig erscheint). Eine weitere Auffrischung nach spätestens zehn Jahren, um die lebenslange Boosterbarkeit aufrechtzuerhalten, erscheint immunologisch (und in Anlehnung an die Erfahrung mit anderen Proteinimpfstoffen) plausibel, ist jedoch nicht evidenzbasiert.
3.1 Epidemiologie
Die Japanische Enzephalitis (JE) gehört zu den häufigsten viralen Erkrankungen in Asien (China,
indischer Subkontinent und Südostasien) mit jährlich etwa 50.000 Erkrankungen, davon ca. 15.000
mit tödlichem Ausgang. Während die Fallzahlen in Ländern wie China, Korea oder Japan infolge
lokaler Impfprogramme deutlich zurückgegangen sind, kann man in den letzten Jahren einen
deutlichen Anstieg von JE in den Bevölkerungen von Bangladesch, Myanmar, Nepal, Thailand, Vietnam und
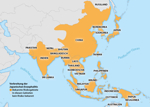
Indonesien verzeichnen (siehe Abb. 3); dabei liegt die Seroprävalenz in den
Hochendemiezonen über
|
Abbildung 3: Verbreitung der Japanischen Enzephalitis
Quelle: modifiziert nach [7] Click on the figure icon to see higher resolution |
Für Reisende aus Nichtendemiegebieten ist das Erkrankungsrisiko mit dem JE-Virus allerdings
generell als niedrig einzustufen. So wurden in einem Review zu den zwischen 1973 und 2008 publizierten Studien in
36 Jahren nur 55 Fälle bei Reisenden aus 17 Ländern gefunden [32].
3.2 Impfstoffe
Der in Europa ab dem 3. Lebensmonat zugelassene und in Österreich verfügbare Impfstoff ist ein mit Aluminium adjuvierter Ganzvirus-Totimpfstoff (Ixiaro®), der den in Verozellen gezüchteten JE-Virusstamm SA14-14-2 (Genotyp III) enthält. Die früher verwendeten (aber nicht in Europa zugelassenen) JE-Impfstoffe, bei denen das Virus auf Mäusehirnen angezüchtet wurde, sind nicht mehr erhältlich.
3.3 Kontraindikationen und Nebenwirkungen
Kontraindikationen sind hohes Fieber und Unverträglichkeiten von Impfstoffbestandteilen. Nur nach sorgfältiger Nutzen-Risiko-Abwägung sollte eine Impfung während der Gravidität oder in der Stillzeit durchgeführt werden (da hierzu keine Daten verfügbar sind).
An Nebenwirkungen sind Kopfschmerzen, Myalgie, gastrointestinale Störungen und Hautveränderungen / lokale Reaktionen zu nennen.
3.4 Impfschema
Das Standardimpfschema mit dem zugelassenen JE-Impfstoff, das sowohl bei Erwachsenen als auch bei Kindern (ab
zwei Monaten) angewandt werden kann, besteht aus zwei Impfungen im Abstand von vier Wochen und einer
Auffrischungsdosis nach zwölf bis 24 Monaten. Nach Boosterung besteht eine Seroprotektionsrate
von nahezu
Nach der empfohlenen Auffrischungsimpfung (nach ein bzw. zwei Jahren) ist laut Fachinformation mit
einem Schutz für zehn Jahre zu rechnen. In einer österreichischdeutschen Studie wurde mittels eines
mathematischen Modells eine Schutzdauer von ca. 14 Jahren nach dem Booster errechnet
[37]. Personen, die mit dem früher verwendeten, aus Maushirn gewonnenen Impfstoff
(JE-MB) eine vollständige Grundimmunisierung erhalten haben, können mit JE-VC problemlos
aufgefrischt werden [38 – 40]. Die mit JE-MB
grundimmunisierten und mit JE-VC geboosterten Personen waren zwei Jahre danach nicht nur gegen den
JE-Impfstamm geschützt; die Seroprotektionsraten gegen Stämme der Genotypen I bis IV lagen
zwischen
3.5 Empfehlungen
- Ein konsequenter Mückenschutz (Abend- und frühe Nachtstunden) mit Repellenzien und Insektizid-behandelten Kleidern ist wichtig.
- Die zugelassenen Impfschemata gegen Japanische Enzephalitis sollten verwendet werden.
- Ist eine Grundimmunisierung nicht abgeschlossen (
d. h. nur eine Impfung), so sollte mit der Grundimmunisierung neu begonnen werden. Sind jedoch bereits zwei Impfungen verabreicht worden, sollte eine dritte Impfung auch nach längerem Intervall (bis zu 10 Jahre) möglich sein (entsprechende Studien dazu fehlen aber). - Nach Grundimmunisierung und einer Boosterung nach zwölf bis 24 Monaten (0 – 28 – 365) ist von einer Impfschutzdauer von (mindestens) zehn Jahren auszugehen.
- Eine Grundimmunisierung bei Personen
> 60 Jahren führt zu deutlich niedrigeren Antiköperspiegeln und einem höheren Prozentsatz von Nonrespondern (47 % ) als bei jüngeren Personen [41]. Ein zusätzlicher konsequenter Mückenschutz ist daher bei älteren Personen besonders wichtig. Eine Auffrischung nach einem Jahr ist bei diesen Personen unbedingt anzuraten [41].
4.1 Epidemiologie
Die Datenlage zur weltweiten Typhusinzidenz ist (besonders auf dem afrikanischen Kontinent) sehr inkomplett, und daher lassen sich nur schwer gesicherte Aussagen treffen [42].
Dennoch kann weltweit eine kontinuierliche Abnahme der gemeldeten Typhusfälle verzeichnet werden, und zwar sowohl bei der absoluten Zahl der Fälle als auch relativ zur Bevölkerungszahl [43]. Die Inzidenz korreliert eng mit dem Zugang zu sauberem Wasser [42].
Der Großteil der Fälle (ca.
Eine Schweizer Studie zeigte eine deutliche Abnahme der Typhusfälle bei Reisenden zwischen 1993 und 2004, wobei das Risiko auf dem indischen Subkontinent am höchsten war [44]. „Visiting Friends and Relatives“ haben im Vergleich zu anderen Reisenden ein etwa zehnmal so hohes Risiko, Typhus zu importieren [45].
In Österreich betrug die Zahl der importierten Typhusfälle zwischen 2007 und 2017 rund zehn pro Jahr, der Großteil davon aus Südasien (die Herkunft wurde allerdings erst ab 2011 im elektronischen Meldeverzeichnis dokumentiert). In dieser Periode trat in Österreich kein Typhus-Todesfall auf [46].
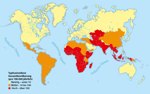
Abb. 4 zeigt eine aktuelle Verbreitungskarte.
|
Abbildung 4: Weltweite Verbreitung von Typhus
Quelle: modifiziert nach [42] Click on the figure icon to see higher resolution |
Oraler Lebendimpfstoff
Der orale Typhus-Lebendimpfstoff enthält Galaktose-Epimerase-defiziente Salmonella typhi 21a und erzeugt vor allem eine lokale Immunität im Darm. Das Impfschema lautet: je eine Gabe an den Tagen 1, 3 und 5 (in den USA ist eine vierte Gabe vorgesehen). Der Schutzeintritt liegt etwa eine Woche nach der dritten Gabe. Die Schutzdauer ist unklar und wird mit einem bis fünf Jahren angegeben. Auch die Schutzrate wird sehr unterschiedlich beurteilt. Zudem kommt es zu Interaktionen mit verschiedenen Malariamedikamenten und mit Antibiotika [47].
In einer Studie aus Chile, Area Occidente, mit den hierzulande erhältlichen magensaftresistenten
Kapseln wurde – bei allerdings sehr niedriger Typhusinzidenz – eine Schutzrate von
Parenteraler Vi-Polysaccharidimpfstoff
Ein i.m. (evtl. auch s.c.) applizierbarer, nicht konjugierter Polysaccharidimpfstoff (
In einem Challenge-Modell verglich eine rezente Studie den zugelassenen, unkonjugierten Polysaccharidimpfstoff
(
4.3 Kontraindikationen und Nebenwirkungen
Der orale Lebendimpfstoff ist bei immunsupprimierten Personen laut Fachinformation kontraindiziert. Es lässt sich jedoch argumentieren, dass der in der Impfung verwendete Stamm Salmonella typhi 21a aufgrund eines induzierten Enzymdefekts keine Galaktose verstoffwechseln und deshalb auch nicht invasiv werden kann. Allerdings wäre die Wirkung der Impfung bei Immunsupprimierten wohl noch schlechter als bei Immunkompetenten.
Folgende Nebenwirkungen werden für den oralen Impfstoff angegeben: gastrointestinale Störungen, Fieber, Kopfschmerzen, Hautveränderungen, Allergien und Schwindel. Der Polysaccharidimpfstoff kann folgende Nebenwirkungen haben: lokale Reaktionen, Fieber, Anaphylaxie, gastrointestinale Störungen, Müdigkeit und vasovagale Synkopen.
4.4 Impfstrategie
Für die Impfempfehlung und die Durchführung (oder Nicht-Durchführung) einer Typhusimpfung gelten folgende drei Überlegungen:
- Die Typhusinzidenz ist bei Reisenden rückläufig und insgesamt sehr gering. In den
D-A-CH -Ländern hat es seit Jahren keinen Todesfall mehr gegeben. - Die Wirksamkeit der derzeit verfügbaren Impfstoffe ist für Reisende nicht gut evaluiert. Sie
zeigen insgesamt jedoch eine sehr bescheidene Effektivität (die allerdings auch nicht geringer ist
als
z. B. jene der Influenzaimpfung). - Typhus ist behandelbar, was allerdings durch vorhandene Antibiotikaresistenzen erschwert wird. Die Auswahl des geeigneten Antibiotikums muss sich nach der lokalen Resistenzsituation richten [50].
Das Für und Wider der Typhusimpfung lässt sich anhand unterschiedlicher Kriterien darstellen.
Kriterium Impfstoff:
- Für die Impfung spricht zunächst die gute Verträglichkeit, der geringe Preis, die hohe Akzeptanz durch Reisende, die Tatsache, dass es sich um eine schwere, hospitalisierungspflichtige Erkrankung handelt, und die Probleme mit der Antibiotikaresistenz.
- Dagegen spricht die insgesamt mäßige Wirksamkeit, der mangelhafte Effektivitätsnachweis bei Reisenden, das Fehlen einer klar definierten Schutzdauer, die Tatsache, dass es sich um eine behandelbare Erkrankung handelt, und der eher geringe Impfbenefit [51].
Kriterium Reiseziel:
- Empfehlung zur Impfung ergeben sich aus Inzidenzraten von Typhuserkrankungen bei Reisenden nach Indien und ostwärts bis einschließlich Papua-Neuguinea, weiters in die ressourcenärmsten Länder Afrikas, und generell eher dann, wenn ländliche Regionen besucht werden.
- Keine Notwendigkeit der Impfung ergibt sich beim Besuch touristisch gut erschlossener Destinationen, wie
z. B. Städtereisen.
Kriterium Reisende:
- Geimpft werden sollten Expats, Personen mit Langzeitaufenthalten im Endemiegebiet, Personen, die unter schlechten hygienischen Bedingungen reisen, „Visiting Friends and Relatives“ sowie Personen unter Protonenpumpenhemmern bzw. mit Achlorhydrie.
- Nicht geimpft werden sollten Touristen (
z. B. Badeaufenthalte, geführte Rundreisen, Städtetourismus) und Geschäftsreisende.
4.5 Empfehlungen
- Insgesamt sollte die Indikation für die Typhusimpfung präziser gestellt werden.
- Eine Impfung ist vorwiegend für den südasiatischen und teilweise für den südostasiatischen Raum absolut vertretbar.
- Die Impfindikation für andere Reiseziele hängt von der Art der Reise und der lokalen Epidemiologie ab.
- Lokale Ausbrüche sollten für die Indikation stärker gewichtet werden (siehe [52]).
- Die eingeschränkte Wirksamkeit der Typhusimpfung muss den Impflingen gegenüber erwähnt werden.
- Lebensmittel-, Wasser- und Händehygiene haben einen bedeutenden Stellenwert in der Prävention des Typhus.
- Konjugatvakzinen werden erst in einigen Jahren in der EU zur Verfügung stehen.
5.1 Epidemiologie
Die fünf humanpathogenen Meningokokken-Serogruppen zeigen sehr unterschiedliche Verbreitungsmuster. In den Industrieländern (inkl. Lateinamerika) herrschen die Serogruppen B und C vor, während im sogenannten afrikanischen Meningitisgürtel vor allem die Serogruppen C, W und X eine Rolle spielen. Die Serogruppe A, die vormals in Afrika vorherrschend war, ist aufgrund von Impfkampagnen deutlich zurückgegangen.
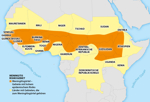
Abbildung 5 zeigt den afrikanischen Meningitisgürtel, der sich von Senegal, Gambia und Guinea-Bissau im Westen des Kontinents bis nach Äthiopien im Osten zieht. Diese Länder haben ein hohes endemisches Risiko, während Länder nördlich und südlich des Gürtels (erweiterter Meningitisgürtel) ebenfalls ein erhöhtes, aber nicht ganz so hohes Risiko aufweisen.
|
Abbildung 5: Der afrikanische Meningitisgürtel
Quelle: modifiziert nach [7] Click on the figure icon to see higher resolution |
Die Länder des Meningitisgürtels zeigen weltweit die höchste Inzidenz an invasiven Meningokokkenerkrankungen. In den Trockenzeiten (Dezember bis Juni) treten dort periodisch, alle fünf bis zwölf Jahre, große Epidemien mit bis zu 1.000 Fällen / 100.000 Einwohner auf, die alle Altersgruppen betreffen. Außerhalb von Epidemien sind vor allem kleine Kinder betroffen.
Hochrisikogebiete können aber auch der Nahe Osten / Arabische Halbinsel, Nordafrika und Ostafrika sein.
Bei Reisen in den Meningitisgürtel sollte die konjugierte, quadrivalente Impfung gegen die Serogruppen A, C, W135 und Y verabreicht werden. Zu beachten ist jedoch auch, dass ein nicht unbeträchtlicher Teil der im Meningitisgürtel auftretenden Meningitiden nicht durch Meningokokken, sondern durch Pneumokokken verursacht wird [53].
Daher ist eine Pneumokokkenimpfung auf jeden Fall für Kinder und ältere Menschen zu erwägen. Weiters lässt sich argumentieren, dass bei relativer Zunahme von Pneumokokken als Meningitiserreger auch Personen außerhalb der genannten Risikogruppen gegen Pneumokokken geimpft werden [53].
Hadj: Die sogenannte Hadj (Pilgerfahrt von Muslimen nach Mekka,
Saudi-Arabien) findet jährlich statt und ist mit ca. zwei Millionen Pilgern die größte
Menschenansammlung der Welt. Es kann dabei zu großen Ausbrüchen an Meningokokkeninfektionen
kommen, die ca. zur Hälfte die lokale Bevölkerung (
Andere Länder: Bei Reisen in Länder abseits des Meningitisgürtels und der Hadj ist eine Meningitisimpfung in der Regel nur dann empfohlen, wenn in diesen Ländern Ausbrüche vorliegen oder besondere Risikofaktoren bestehen. Kinder und Jugendliche sollten nach den Empfehlungen des Österreichischen Impfplans geimpft sein, wobei auch die Empfehlungen des Reiselands zu beachten sind. Was die Wirksamkeit der Impfung betrifft, liegen Daten bis zu fünf Jahren vor – deshalb sollten bei entsprechendem Expositionsrisiko Boosterungen alle fünf Jahre durchgeführt werden.
Tabelle 2 zeigt weitere Faktoren, die das Risiko für Meningokokkenerkrankungen beeinflussen.
|
Tabelle 2: Risikofaktoren für Meningokokkenerkrankungen
|
Massenveranstaltungen: Bestimmte Massenveranstaltungen (mit
per definitionem mehr als 1.000 Teilnehmern) wie
Reiseunabhängige Impfempfehlung:
Colleges und Universitäten: Nach den Ländern des
Meningitisgürtels und der Hadj ist die dritthäufigste Ursache von Meningokokkeninfektionen
weltweit bereits der Aufenthalt in Schlafsälen von Gemeinschaftseinrichtungen
(
Risikogruppe Homosexuelle / MSM: Die nasopharyngeale Besiedelung mit Meningokokken ist bei Männern, die Sex mit Männern haben (MSM), häufiger als bei heterosexuellen Männern. Auch urethrale und rektale Kolonisationen wurden beobachtet. Meningokokkenausbrüche (Serogruppe C) unter MSM wurden seit 2001 aus nordamerikanischen Städten gemeldet. In Folge führten dort viele Großstädte kostenlose Impfaktionen für diese Risikogruppe, auch für Nichtversicherte, ein.
Auch in Europa gab es 2013 derartige Ausbrüche in MSM-Communities, etwa in Paris, in Belgien oder in Berlin. Aus den Niederlanden und Großbritannien wurden keine solchen Ausbrüche berichtet, was möglicherweise mit den guten Durchimpfungsraten zusammenhängt.
Die quadrivalente Impfung, aber auch die Impfung gegen Serogruppe B ist für MSM mit Risikoverhalten zu empfehlen. Aufgrund der hohen genetischen Homologie zwischen Neisseria meningitidis und N. gonorrhoeae könnte es durch Impfung gegen Gruppe-B-Meningokokken (4CmenB – Bexsero®) auch zu reduzierten Raten an Gonorrhoe kommen [56].
Risikogruppe Immunsupprimierte / HIV: HIV-positive Personen
haben ein um den Faktor
HIV-positiven Reisenden sollte die Impfung (bevorzugt gegen A / C / W135 / Y und B) jedoch angeboten werden.
5.2 Impfstoffe
Es gibt neben den monovalenten Impfstoffen gegen die Serogruppen C (und A, dies aber nicht in Europa) seit einigen Jahren tetravalente Impfstoffe gegen die Serogruppen A, C, W135 und Y (Nimenrix®, Menveo®). Es handelt sich dabei um Totimpfstoffe, die an ein Trägerprotein gekoppelte Kapselpolysaccharide der Erreger enthalten.
Weiters gibt es nun auch Impfstoffe gegen Meningokokken Serogruppe B (Bexsero®, Trumenba®), bei denen es sich (im Unterschied zu den gegen die anderen Serogruppen gerichteten Polysaccharidimpfstoffen) um Proteinimpfstoffe handelt.
5.3 Kontraindikationen und Nebenwirkungen
Kontraindikationen sind nicht beschrieben.
Impfstoffe gegen Serogruppen A, C, W135, Y: Lokale Reaktionen, Appetitlosigkeit, Reizbarkeit, Schläfrigkeit, Kopfschmerzen, Magen / Darm, Haut, Fieber, Müdigkeit, psychogene Reaktionen.
Impfstoffe gegen Serogruppe B: lokale Reaktionen, Kopfschmerzen, Müdigkeit, Muskel- oder Gelenkschmerzen, Schüttelfrost, Fieber, Essstörungen, ungewöhnliches Schreien, Krämpfe, Diarrhö, Erbrechen, Hautausschläge und psychogene Reaktionen.
5.4 Impfstrategie
Die tetravalenten Impfstoffe gegen die Serogruppen A, C, W135 und Y werden bei Kindern ab zwei Jahren (bei Nimenrix® laut Fachinformation ab der 6. Lebenswoche), Jugendlichen und Erwachsenen als Einzeldosis i.m. verabreicht.
Bexsero® wird (außer bei Kindern unter fünf Monaten) als zwei Einzeldosen im Abstand von mindestens einem Monat gegeben, eine Auffrischung ist derzeit nicht vorgesehen.
Für Trumenba® existieren zurzeit zwei Schemata (zugelassen ab 10 Jahren): entweder zwei Dosen im Abstand von sechs Monaten oder drei Dosen (zwei im Abstand von einem Monat und eine dritte Dosis vier Monate später). Nach beiden Schemata sollte bei bestehendem Risiko einer invasiven Meningokokkenerkrankung eine Auffrischungsimpfung in Betracht gezogen werden. Bexsero® und Trumenba® sind nicht austauschbar verwendbar.
5.5 Empfehlungen
- Alle Kinder und Jugendlichen sollten gemäß dem Österreichischen Impfplan gegen Meningokokken geimpft werden.
- Als Reiseimpfung ist die Meningokokkenimpfung (gegen
A / C / W135 / Y und B) für Reisende in
Hochrisikogebiete wie
z. B. Saudi-Arabien (Hadj – hier ist die Impfung verpflichtend), den afrikanischen Meningitisgürtel und in Länder mit aktuellen Ausbrüchen zu empfehlen. (In diesem Kontext sollte auch an Jugendliche und junge Erwachsene gedacht werden, die für eine gewisse Zeit im Kontext von Hilfs- und Sozialprojekten nach Afrika reisen.) - Weiters sind Impfungen gegen Meningokokken (A / C / W135 / Y
und B) zu erwägen:
- In Gebieten mit mittlerem Risiko bei Gegebenheiten, die mit einer Risikoerhöhung einhergehen. Dazu gehören: langer Aufenthalt, viel Kontakt mit lokaler Bevölkerung, Kontakt mit großen Menschenansammlungen.
- In Gebieten mit allgemein niedrigem Risiko falls
- Umstände mit höherer Infektionswahrscheinlichkeit bestehen. Dazu gehören Jugendliche an Universitäten oder in Studentenheimen, besonders im angloamerikanischen Raum, Massenveranstaltungen und sexuelles Risikoverhalten (MSM).
- Bei Personen, bei denen individuell eine erhöhte Anfälligkeit besteht durch
angeborene oder erworbene Erkrankungen wie
z. B. Asplenie, gewisse Immundefekte, HIV-Infektion, chronische Erkrankungen, die mit Immunsuppression einhergehen, und Nikotinabusus.
Interessenkonflikte
Alle Autoren haben unentgeltlich an diesem Projekt mitgearbeitet.
- Ursula Wiedermann: In den letzten fünf Jahren: Wissenschaftliche Kooperationsprojekte (an der MedUniWien, PhaseIII / IV-Studien) mit Pfizer, Novartis / GSK, Themis, Imugene. Scientific Officer / Scientific Advisory Board von Imugene (Biotech Australia).
- Herwig Kollaritsch: In den letzten fünf Jahren – Vorträge zu Impfthemen ohne Produktbezug – finanziert von Sanofi Pasteur, MSD, Pfizer.
- Andrea Grisold: In den letzten fünf Jahren – keine.
- Christoph Hatz: In den letzten fünf Jahren: von der Firma Novartis / später GSK sowie Takeda finanzierte Vakzine-Studien. Vorträge zu reisemedizinischen Themen ohne Produktbezug, finanziert von Spirig, Bayer, Sanofi Pasteur MSD, und GSK. Keine Übernahme der Kosten für Kongressreisen und Tagungsgebühren von wissenschaftlichen Veranstaltungen.
- Ursula Hollenstein: In den letzten fünf Jahren Vorträge und schriftliche Beiträge zu Impfthemen und Reisemedizin ohne Produktbezug, finanziert von Eli Lilly, Valneva, Fresenius Kabi.
- Heidemarie Holzmann: In den letzten fünf Jahren – Vorträge, die Impfthemen inkludierten, organisiert von Roche und DiaSorin.
- Maria Kitchen: In den letzten fünf Jahren – keine.
- Ingomar Mutz: Honorar für Vorträge zu Impfthemen (Baxter, Novartis, Sanofi Pasteur MSD, Wyeth / Pfizer und GSK); Honorar für Beratungstätigkeit als Mitglied von Data Safety Monitoring Committees (Baxalta, CureVac, Pfizer).
- Florian Thalhammer: In den letzten fünf Jahren – keine.
- Angelika Wagner: In den letzten fünf Jahren – keine.
- Günter Weiss: In den letzten fünf Jahren – keine.
- Christoph Wenisch: In den letzten fünf Jahren – keine.
Literatur
-
Yellow Fever Situation Report.
30th June 2016. https://www.who.int/emergencies/yellow-fever/situation-reports/30-june-2016/en/

-
Epidemiological Alerts and Updates.
https://www.paho.org/hq/index.php?option=com_content&view=article&id=1239:2009-epidemiological-alerts-updates&Itemid=2291&lang=en

-
Global yellow fever vaccination coverage from 1970 to 2016: an adjusted retrospective analysis.
Lancet Infect Dis,
2017; 17(11):1209–1217.


-
Yellow Fever – Americas (24): Germany ex Brazil (Rio de Janeiro).
ProMED-mail post 27 Mar 2018. http://www.promedmail.org

-
Yellow Fever – Americas (34): Switzerland ex French Guiana.
ProMED-mail post 15 Aug 2018. http://www.promedmail.org

-
Increased risk of yellow fever infections among unvaccinated European travellers due to ongoing outbreak in Brazil, July 2017 to March 2018.
Euro Surveill,
2018; 23(11).


-
Yellow Book 2018.
https://www.cdc.gov/features/yellowbook/index.html

-
Case report: probable transmission of vaccine strain of yellow fever virus to an infant via breast milk.
CMAJ,
2011; 183(4):E243–E245.


-
Adverse event reports following yellow fever vaccination, 2007–13.
J Travel Med,
2016; 23(5): taw045.


-
Yellow Fever Vaccine Booster Doses: Recommendations of the Advisory Committee on Immunization Practices, 2015.
MMWR Morb Mortal Wkly Rep,
2015; 64(23):647–650.
https://www.cdc.gov/mmwr/preview/mmwrhtml/mm6423a5.htm


-
Grading of recommendations, assessment, development, and evaluation (GRADE) for yellow fever vaccine booster doses.
https://www.cdc.gov/vaccines/acip/recs/grade/yf-vac-boost.pdf

-
Implementation of the International Health Regulations (2005).
http://apps.who.int/gb/ebwha/pdf_files/WHA67/A67_R13-en.pdf

-
Background Paper on Yellow Fever Vaccine.
http://www.who.int/immunization/sage/meetings/2013/april/1_Background_Paper_Yellow_Fever_Vaccines.pdf

-
Statement on the Use of Booster Doses of Yellow Fever Vaccine.
https://www.canada.ca/en/public-health/services/publications/diseases-conditions/use-booster-doses-yellow-fever-vaccine.html

-
Assessment of IgG antibodies against yellow fever virus after vaccination with 17D by different assays: neutralization test, haemagglutination inhibition test, immunofluorescence assay and ELISA.
Trop Med Int Health,
1999; 4(12):867–871.


-
Persistence of yellow fever virus-specific neutralizing antibodies after vaccination among US travellers.
J Travel Med,
2018; 25(1):tay108.


- Plotkin’s Vaccines. 7th ed. Philadelphia, PA: Elsevier; 2018. ISBN 978-0-3233-5761-6 (hardcover).
-
Duration of post-vaccination immunity against yellow fever in adults.
Vaccine,
2014; 32(39):4977–4984.


-
Demographic profile of sylvatic yellow fever in Brazil from 1973 to 2008.
Trans R Soc Trop Med Hyg,
2013; 107(5):324–327.


-
Booster dose after 10 years is recommended following 17DD-YF primary vaccination.
Hum Vaccin Immunother,
2016; 12(2):491–502.


-
Rabies – Epidemiology and burden of disease.
https://www.who.int/rabies/epidemiology/en/

-
Rabies vaccines; WHO position paper – April 2018.
https://www.who.int/rabies/resources/who_wer9316/en/

-
Human rabies. 2016 updates and call for data.
https://www.who.int/rabies/resources/who_wer9207/en/

-
Rabies vaccines and immunoglobulins: WHO position.
https://www.who.int/rabies/resources/who_cds_ntd_nzd_2018.04/en/

-
Pre-exposure intradermal rabies vaccination: a non-inferiority trial in healthy adults on shortening the vaccination schedule from 28 to 7 days.
Clin Infect Dis,
2018; ciy513 [Epub ahead of print].


-
Survival of neutralizing antibody in previously rabies vaccinated subjects: a prospective study showing long lasting immunity.
Vaccine,
2006; 24(18):3878–3880.


-
Immunogenicity study of abbreviated rabies preexposure vaccination schedules.
J Travel Med,
2007; 14(3):173–176.


-
Rabies Antibody Response After Booster Immunization: A Systematic Review and Meta-analysis.
Clin Infect Dis,
2018; 67(12):1932–1947.


-
Single visit rabies pre-exposure priming induces a robust anamnestic antibody response after simulated post-exposure vaccination: results of a dose-finding study.
J Travel Med,
2017; 24(5):tax033.


-
One clinic visit for pre-exposure rabies vaccination (a preliminary one year study).
Vaccine,
2012; 30(19):2918–2920.


-
Kommentar des Schweizerischen Expertenkomitees für Reisemedizin: Neues Tollwutimpfschema in der Reisemedizin.
Swiss Med Forum,
2018; 18(32):626–627.

-
Japanese encephalitis in travelers from non-endemic countries, 1973–2008.
Am J Trop Med Hyg , 2010; 82(5):930–936.

-
Short-Term Immunogenicity and Safety of an Accelerated Pre-Exposure Prophylaxis Regimen With Japanese Encephalitis Vaccine in Combination With a Rabies Vaccine: A Phase III, Multicenter, Observer-Blind Study.
J Travel Med,
2015; 22(4):25–231.


-
One-year immunogenicity kinetics and safety of a purified chick embryo cell rabies vaccine and an inactivated Vero cell-derived Japanese encephalitis vaccine administered concomitantly according to a new,
1-week , accelerated primary series. J Travel Med, 2016; 23(3):taw011.

-
Comparison of a single, high-dose vaccination regimen to the standard regimen for the investigational Japanese encephalitis vaccine, IC51: a randomized, observer-blind, controlled Phase 3 study.
Vaccine,
2009; 27(15):2188–2193.


-
Long-term immunity and immune response to a booster dose following vaccination with the inactivated Japanese encephalitis vaccine IXIARO, IC51.
Vaccine,
2010; 28(32):5197–5202.


-
Persistence of antibodies six years after booster vaccination with inactivated vaccine against Japanese encephalitis.
Vaccine,
2015; 33(30):3600–3604.


-
A single dose of vero cell-derived Japanese encephalitis (JE) vaccine (Ixiaro) effectively boosts immunity in travelers primed with mouse brain-derived JE vaccines.
Clin Infect Dis , 2012; 55(6):825–834.

-
Immunogenicity of one dose of Vero cell culture-derived Japanese encephalitis (JE) vaccine in adults previously vaccinated with mouse brain-derived JE vaccine.
Vaccine,
2012; 30(20):3090–3096.


-
Cross-protection elicited by primary and booster vaccinations against Japanese encephalitis: a two-year follow-up study.
Vaccine,
2013; 32(1):119–123.


-
Age-related differences in humoral and cellular immune responses after primary immunisation: indications for stratified vaccination schedules.
Sci Rep,
2018; 8(1):9825.


-
Burden of typhoid fever in low-income and middle-income countries: a systematic, literature-based update with risk-factor adjustment.
Lancet Glob Health,
2014; 2(10):e570–e580.


-
SAGE Meeting of October 2017.
https://www.who.int/immunization/sage/meetings/2017/october/presentations_background_docs/en/

-
Imported typhoid fever in Switzerland, 1993 to 2004.
J Travel Med,
2008; 15(4):248–251.


-
Imported enteric fever: case series from the hospital for tropical diseases, London, United Kingdom.
Am J Trop Med Hyg , 2010; 82(6):1121–1126.

- 2018.
-
Fachinformation Vivotif Kapseln.
https://aspregister.basg.gv.at/document/servlet?action=show&zulnr=2-00011&type=DOTC_FACH_INFO

-
Immunogenicity, efficacy and serological correlate of protection of Salmonella typhi Vi capsular polysaccharide vaccine three years after immunization.
Vaccine,
1996; 14(5):435–438.


-
Efficacy and immunogenicity of a Vi-tetanus toxoid conjugate vaccine in the prevention of typhoid fever using a controlled human infection model of Salmonella Typhi: a randomised controlled, phase 2b trial.
Lancet,
2017; 390(10111):2472–2480.


-
Extensively Drug-Resistant Typhoid — Are Conjugate Vaccines Arriving Just in Time?
N Engl J Med , 2018; 379(16):1493–1495.

-
Statementon International Travellers and Typhoid.
http://publications.gc.ca/collections/collection_2014/aspc-phac/HP40-98-2014-eng.pdf

-
Disease Outbreak News (DONs).
https://www.who.int/csr/don/en/

-
Global etiology of bacterial meningitis: A systematic review and meta-analysis.
PLoS One,
2018; 13(6):e0198772.


-
Meningococcal disease burden and transmission in crowded settings and mass gatherings other than Hajj / Umrah: A systematic review.
Vaccine,
2018; 36(31):4593–4602.


-
Use of Serogroup B Meningococcal Vaccines in Adolescents and Young Adults: Recommendations of the Advisory Committee on Immunization Practices, 2015.
MMWR Morb Mortal Wkly Rep,
2015; 64(41):1171–1176.


-
Effectiveness of a group B outer membrane vesicle meningococcal vaccine against gonorrhoea in New Zealand: a retrospective case-control study.
Lancet,
2017; 390(10102):1603–1610.


-
Recommendations for Use of Meningococcal Conjugate Vaccines in HIV-Infected Persons – Advisory Committee on Immunization Practices, 2016.
MMWR Morb Mortal Wkly Rep,
2016; 65(43):1189–1194.



|
|
published online:
|
| english abstract |